微泡介导超声如何用“物理之力”重塑实体瘤免疫格局?
HUIYING
微泡介导的聚焦超声技术概述
微泡介导的聚焦超声技术的提出,是为了克服传统聚焦超声在细胞层面作用效率低、选择性差的核心局限。传统的聚焦超声单独作用时,主要依靠热效应或较弱的空化效应,难以在单细胞精度上实现可控的、可逆的膜穿孔,更无法有效将声能转化为精准的机械信号去调控免疫细胞功能。而通过引入微泡作为“能量放大器”和“机械力转化器”,超声的声能被高效地传递给微泡,驱动其发生稳定或惯性空化,从而将宏观的声能转化为局部的微射流、剪切力和冲击波。这一“介导”过程不仅能在保持细胞活力的前提下,可逆地打开细胞膜通道(实现大分子药物靶向递送),还能通过机械力传导激活细胞内信号通路(如钙内流、NF-κB通路),直接调控免疫细胞的分泌功能(如细胞因子谱重塑),最终实现对免疫细胞“递送+调控”的双重精准干预。
这一策略之所以成为实体瘤免疫治疗的新方向,关键在于它同时解决了传统疗法在实体瘤中面临的两大核心困境:药物/细胞难以进入肿瘤核心的物理屏障问题,以及即使进入也会被肿瘤微环境“缴械”的功能抑制问题。通过单一技术平台,该策略既能作为“增效器”增强CAR-T细胞和免疫检查点抑制剂的疗效(如利用超声打开细胞膜递送增效药物,同时通过机械刺激激活T细胞功能),又能作为独立的“原位疫苗”疗法在肿瘤局部诱导免疫应答(如通过惯性空化释放肿瘤抗原,同时调控免疫细胞分泌趋化因子招募更多效应细胞)。这种“改造战场”而非仅“增兵”的物理-免疫联合干预思路,为攻克实体瘤免疫治疗难题提供了全新的策略方向。
HUIYING
微泡介导的聚焦超声与传统聚焦超声(tFUS)
的区别
| 对比维度 | 传统聚焦超声(tFUS) | 微泡介导的聚焦超声(MB-FUS) |
| 作用机制 | 主要依赖超声的热效应和机械效应(如空化,但无外源空化核) | 依赖微泡作为空化核,增强机械效应,产生稳定或惯性空化 |
| 细胞膜影响 | 通常不直接导致细胞膜穿孔,主要通过热效应影响细胞 | 可诱导可逆的细胞膜穿孔(声孔效应),促进大分子进入 |
| 靶向递送能力 | 药物递送依赖热敏脂质体等载体,效率有限 | 可与微泡结合递送药物/基因,局部释放效率高 |
| 免疫调节作用 | 可通过热效应改变肿瘤微环境,但对免疫细胞直接调节研究较少 | 可直接调节免疫细胞分泌谱,影响多种细胞因子和趋化因子 |
| 临床应用 | 已用于肿瘤消融、血脑屏障开放等 | 正在探索用于免疫治疗、药物递送、基因治疗等 |
HUIYING
微泡介导的聚焦超声技术实现过程
本研究采用的实验装置和流程如图1所示。具体步骤如下:
细胞准备:使用人Jurkat T细胞系或新鲜分离的人外周血单个核细胞(PBMCs)。部分实验中将细胞激活(如用抗CD3/CD28抗体)以模拟体内状态。
微泡加入:在细胞悬液中加入临床级微泡Definity(细胞与微泡比例约1:217),确保均匀混合。
超声处理:将样品置于37°C恒温水槽中的样品室内,样品室两侧为Mylar薄膜以便超声穿透。使用1 MHz聚焦超声换能器,发射1000个周期、脉冲重复间隔5 ms(占空比20%),声压范围为208–563 kPa,持续2分钟。同时,用3.5 MHz被动换能器记录微泡散射信号,以监测空化行为(稳定空化/惯性空化)。
检测分析:处理后,细胞经洗涤、染色,用流式细胞术分析膜通透性(FITC-葡聚糖摄取)和细胞活力(PI排除)。部分实验收集上清液,用Luminex技术检测96种细胞因子/趋化因子的分泌变化。
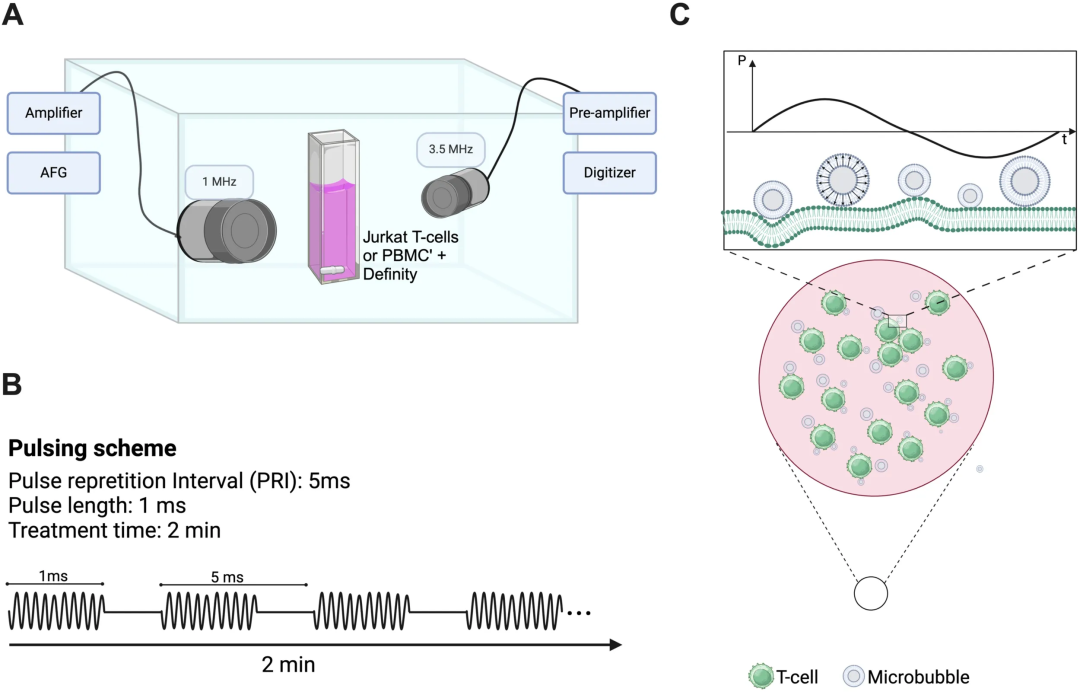
图1:定制超声处理装置与实验方案
图1展示了整个实验的核心装置构成和操作流程。
图1A描绘了一个恒温(37°C)水槽,其中央放置一个带有Mylar薄膜窗口的样品室,样品室两侧共焦对准两个换能器:一个1 MHz的治疗超声换能器(用于施加超声)和一个3.5 MHz的被动空化检测换能器(用于记录微泡散射信号)。细胞悬液、Definity微泡以及FITC-葡聚糖(实验中用于检测通透性)被混合在样品室内,并通过磁力搅拌子保持均匀分布。
图1B以脉冲序列图的形式展示了超声处理参数:频率1 MHz,1000个周期,脉冲重复间隔5 ms,占空比20%,声压范围为208-563 kPa,总处理时间2分钟。
图1C是一个原理示意图,形象地解释了微泡在超声场中振动,并作用于邻近免疫细胞(如T细胞)的过程,即声孔效应的基础。
HUIYING
临床研究
研究方法
T细胞:适应性免疫的核心细胞(CD4+辅助、CD8+杀伤),肿瘤免疫治疗的主要靶点;PBMCs:外周血单个核细胞混合群体,含T细胞、B细胞、NK细胞、单核细胞,更接近体内免疫环境;PBMCs包含T细胞;T细胞是单一类型,PBMCs是混合群体Jurkat T细胞用于参数优化和机制验证;PBMCs用于临床相关性验证和免疫功能调控研究,两者形成从简单到完整的递进研究链条
细胞来源:健康志愿者外周血分离的PBMCs,以及Jurkat T细胞系。
实验分组:不同声压(208、416、563 kPa)处理组,以及未超声的假处理组(Sham)。
检测指标:
膜通透性与活力:流式细胞术(FITC-葡聚糖、PI染色),并区分T细胞亚群(CD3、CD4)。
微泡空化行为:被动空化检测,分析谐波和宽带发射。
细胞因子分泌:Luminex 96重检测,在3h、6h、12h、24h、48h收集上清液。
蛋白相互作用与通路分析:使用STRING数据库和KEGG通路富集。
研究结果
超声增强T细胞膜通透性并保持高活力
Jurkat T细胞:图2显示,随着声压增加,未激活和激活的Jurkat细胞中摄取FITC-葡聚糖的细胞比例显著上升,在563 kPa时分别达到41%和31%,细胞活力仍保持在80%以上(图2C–F)。
图2:超声辅助Jurkat T细胞大分子递送的效率与活力
图2通过流式细胞术定量评估了超声对Jurkat T细胞的影响。
图2A-B展示了门控策略:假处理组(A)无FITC摄取,而563 kPa处理组(B)出现FITC阳性且PI阴性的“可存活且被通透的细胞”。
图2C-D显示,未激活Jurkat细胞中,可存活通透细胞比例随声压从208 kPa增至563 kPa而显著提升至41.0%(p<0.0001),细胞活力始终保持在83.8%-100%。
图2E-F表明,激活的Jurkat细胞呈现相似趋势,563 kPa时通透率达31.1%(p<0.001),活力为83.5%。综上,无论细胞激活状态如何,超声均能在保持高活力的前提下,有效增强Jurkat T细胞的膜通透性。
PBMCs:图3A表明,PBMCs中总细胞摄取率在563 kPa时达29.4%,且细胞活力维持在96%以上(图3C)。进一步分析T细胞亚群(图3B),CD3+细胞在563 kPa时摄取率为31.6%,CD4+和CD8+(以CD3+CD4-代表)分别达26.0%和13.7%,各亚群比例在超声后无明显变化(图3D),说明超声无选择性杀伤。
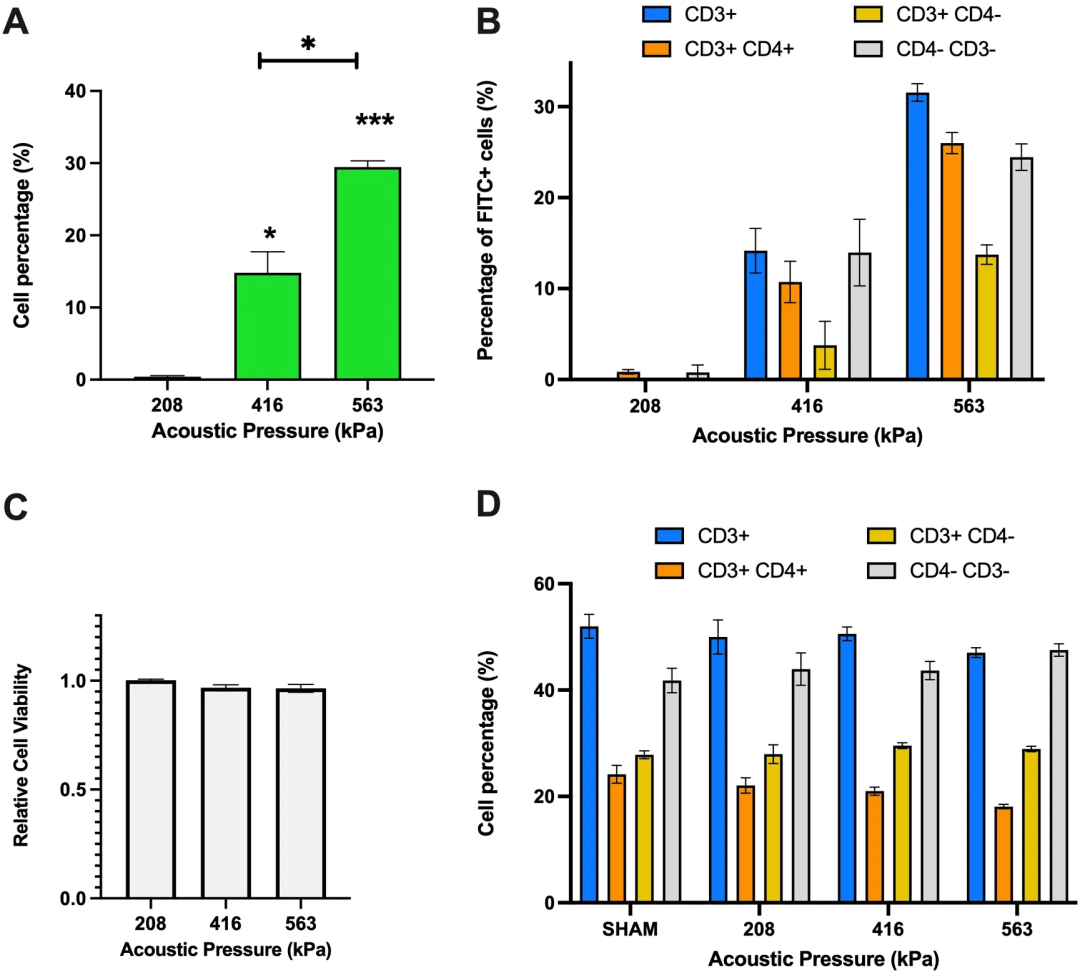
图3:超声辅助新鲜分离人PBMCs的通透效率与活力分析
图3展示了超声对新鲜分离人PBMCs的影响。
图3A显示,总细胞中可存活且被通透的比例随声压升高而显著增加,563 kPa时达29.4%(p<0.01)。
图3B分析T细胞亚群:CD3+细胞通透率为31.6%,CD3+CD4+、CD4-CD3-和CD3+CD4-(CD8+替代标志)分别为26.0%、24.5%和13.7%,表明超声可有效作用于多种免疫细胞。
图3C-D显示,所有声压下细胞活力均维持在96%-100%,各亚群比例稳定,无选择性损伤。综上,超声能在保持高活力的前提下高效通透新鲜人免疫细胞,且原代细胞耐受性优于Jurkat细胞系。
微泡空化行为与声压相关
图4展示了被动空化检测结果:随着声压升高,谐波和宽带发射增强,表明微泡从稳定空化过渡到惯性空化(破裂)。
图4E和4F量化了宽带发射积分和累积惯性空化剂量,证实较高声压下微泡破裂更显著。
图4:被动空化检测与微泡行为分析
图4通过被动空化检测揭示了不同声压下微泡的物理行为。
图4A显示,随着声压升高,微泡回波信号中出现宽带发射(微泡破裂的标志)。
图4B-D的时频分析进一步表明,208 kPa时以稳定空化为主,而416 kPa和563 kPa时出现显著的惯性空化(破裂)。
图4E-F量化了宽带发射积分和累积惯性空化剂量,证实声压越高,微泡破裂越剧烈。综上,声压通过调控微泡空化行为(稳定空化→惯性空化),决定了细胞膜通透效率的物理基础。
超声调节免疫细胞分泌谱,呈时间与压力依赖性
图5A为蛋白相互作用网络图,显示受影响的细胞因子间存在复杂联系。
图5B统计了主要通路中受调节的蛋白数量,TNF信号通路(14种)和NF-κB通路(11种)最为显著。
图5C热图展示了所有显著变化的细胞因子在不同时间点和声压下的表达倍数变化(红色为上调,绿色为下调)。变化幅度从0.06倍(IL-13,6h)至3.8倍(IL-1α,3h)。较高声压(563 kPa)引起更广泛的调节,且早期以上调为主,后期以下调为主。
图5D和5E分别聚焦于TNF和NF-κB通路中的因子变化,显示IL-1β、TNF-α等在563 kPa下显著下调。
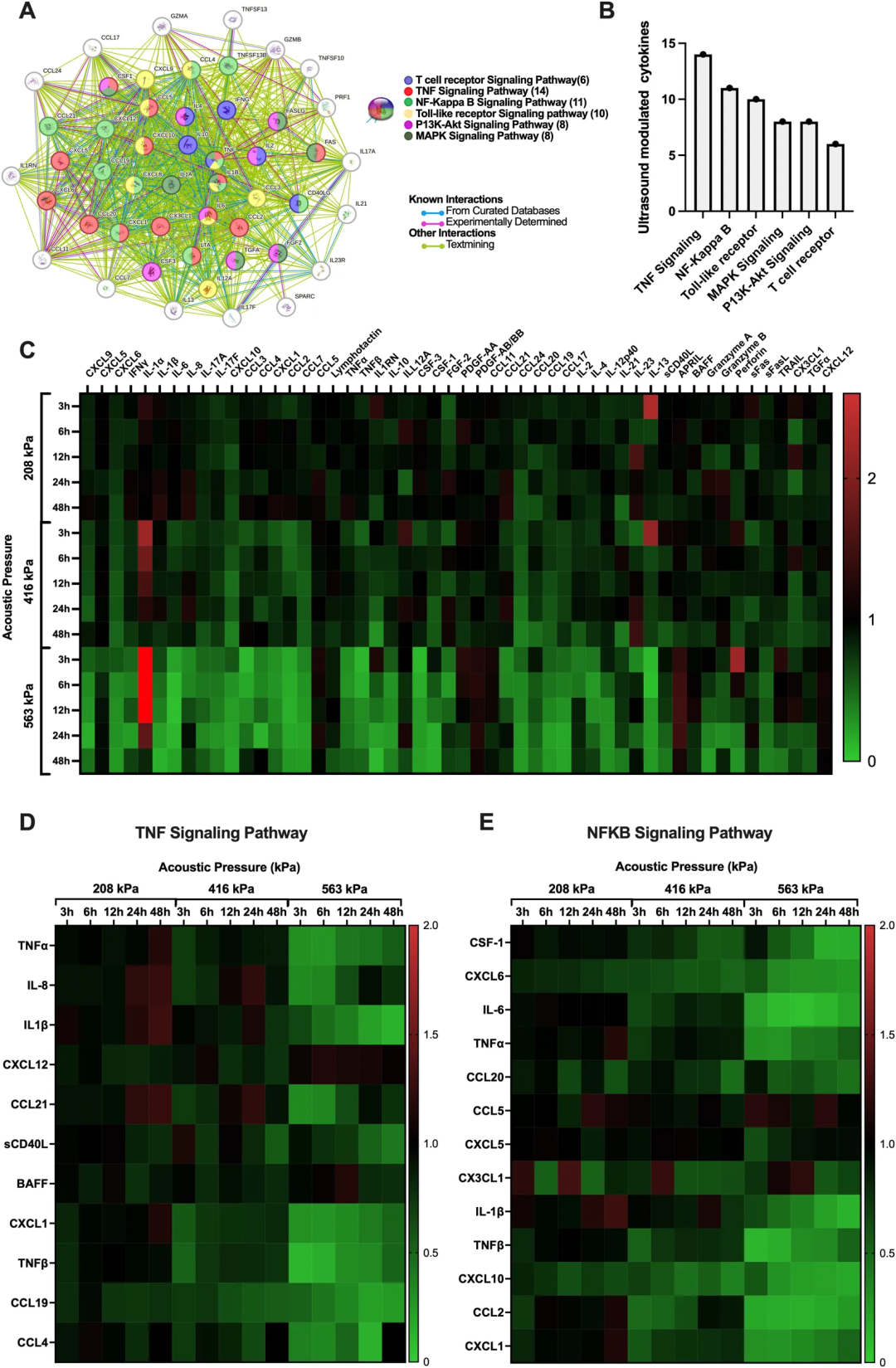
图5:超声对PBMCs分泌谱的整体影响与通路分析
图5全景式展示了超声处理后PBMCs分泌谱的时空变化及其参与的生物学通路。
图5A的蛋白互作网络显示,受调节的细胞因子之间存在复杂的功能联系;
图5B的统计表明,TNF信号通路(14种)和NF-κB通路(11种)是受影响最显著的两条通路。
图5C的全局热图揭示了分泌变化的三个关键特征:时间依赖性(3-48小时持续变化)、压力依赖性(声压越高变化越显著)和双向调节性(同一因子在不同时间点可上调和下调)。
图5D-E分别聚焦TNF和NF-κB通路,展示了IL-1β、TNF-α等关键因子的具体变化模式。综上,超声通过调控多条免疫相关通路,实现了对PBMCs分泌谱的精准、动态调节
膜通透性与细胞因子分泌呈负相关趋势
图6将细胞因子分泌与PBMCs膜通透性进行关联分析,显示多数因子在3h、12h、48h时与通透性呈负相关(如IL-1β、TNF-α、TNF-β),部分具有统计学显著性(表1)。提示膜穿孔可能暂时抑制细胞分泌功能。
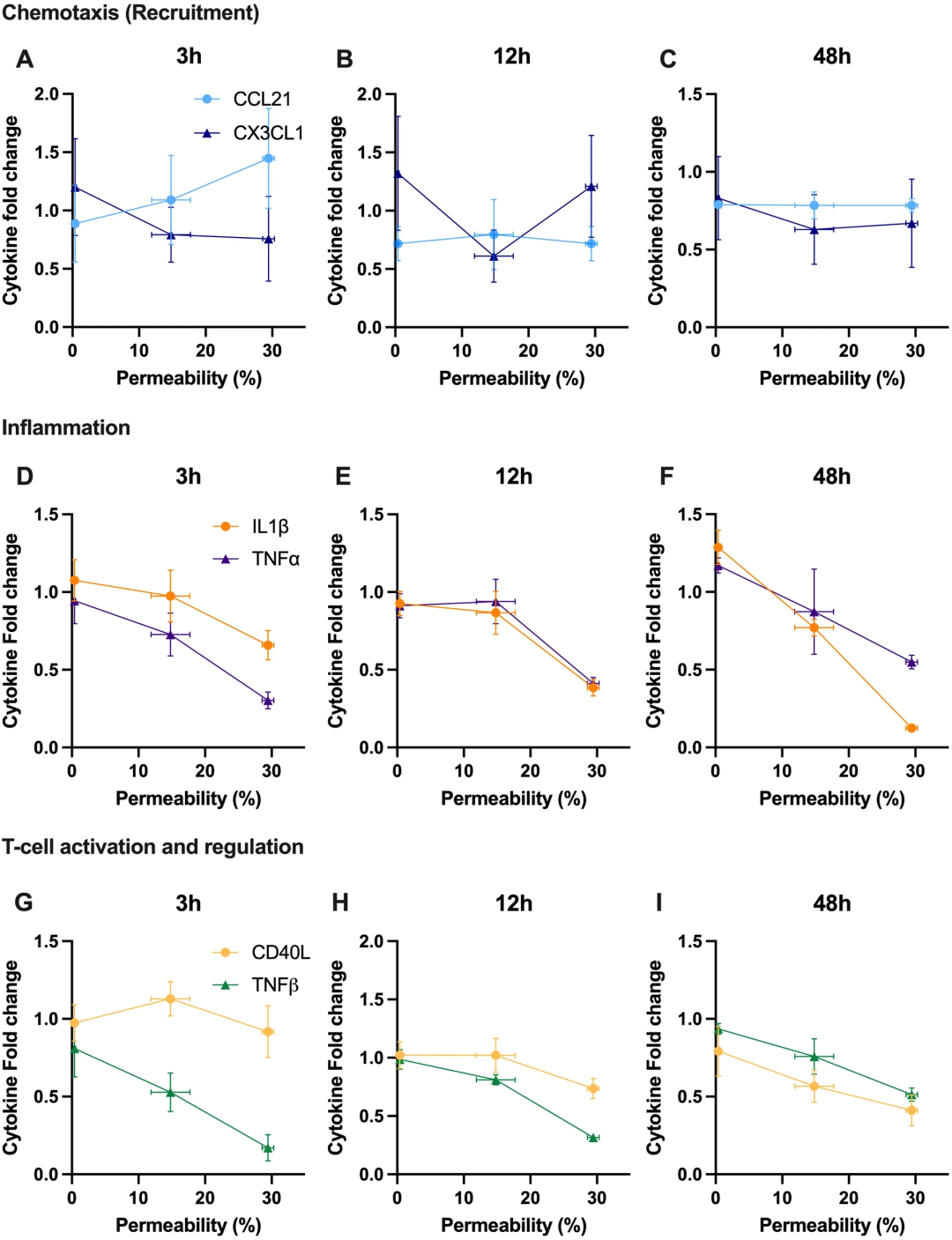
图6:细胞膜通透性与细胞因子分泌的相关性分析
图6将超声诱导的细胞膜通透性与细胞因子分泌变化直接关联,揭示了二者之间的关系。
图6A-C显示趋化因子(CCL21、CX3CL1)的分泌随通透性增加多呈下降趋势;
图6D-F表明炎症因子(TNF-α、IL-1β)与通透性呈显著负相关,尤其IL-1β在48小时最为明显;
图6G-I展示T细胞调节因子(TNF-β、sCD40L)同样以负相关为主。结合表1的统计分析,多数因子的负相关具有统计学意义。综上,超声诱导的膜穿孔效应在成功递送药物的同时,可能短期内抑制细胞的蛋白质合成与分泌功能。
HUIYING
总结
本研究首次系统评估了微泡介导的聚焦超声对人T细胞及PBMCs的免疫调节作用。主要发现包括:
超声可在保持细胞高活力的前提下,显著提高T细胞膜通透性,为药物递送提供新途径。
超声处理诱导了时间与压力依赖性的细胞因子/趋化因子分泌变化,涉及TNF、NF-κB等关键免疫通路,调节了IL-1β、TNF-α、CCL21等多种抗肿瘤相关因子。
膜通透性与细胞因子分泌多呈负相关,提示机械穿孔可能短暂抑制分泌,需进一步优化参数以平衡递送效率与免疫调节效果。
综上,微泡介导的聚焦超声作为一种非侵入性、可调控的技术,兼具药物递送与免疫调节双重功能,为实体瘤的免疫治疗提供了新的策略方向。未来需在体内模型中验证其疗效,并探索与免疫检查点抑制剂或CAR-T疗法的联合应用。
2026-03-05 11:43:25
目录 返回
首页
